
“微信扫一扫”进入"可可试卷"微信小程序刷题
执业药师《药学专业知识一》历史真题(1317题)
第561题
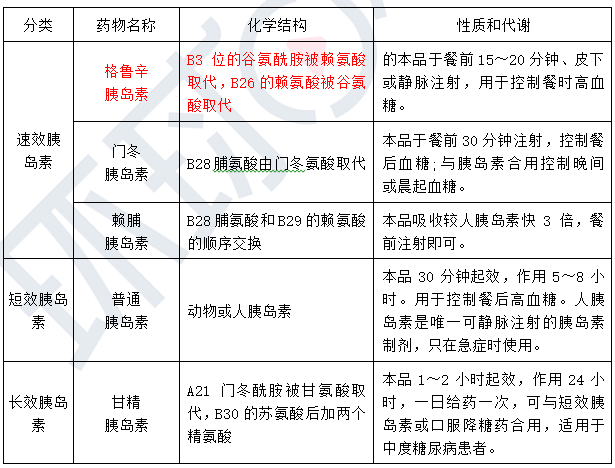
某胰岛素类药物系由胰岛素化学结构B链3位的谷氨酰胺被赖氨酸取代,B链26位的赖氨酸被谷氨酸取代而成,该药物是
A.门冬胰岛素
B.赖脯胰岛素
C.格鲁辛胰岛素
D.甘精胰岛素
E.猪胰岛素
参考答案:C
解析:
本题考查的是胰岛素及其类似物。
格鲁辛胰岛素系由胰岛素化学结构B链3位的谷氨酰胺被赖氨酸取代,B链26位的赖氨酸被谷氨酸取代而成。
【考点延展】
第562题
当原料药粒径较大时,进食时比空腹的Cmax、AUC都大,说明
A.进食比空腹的胃排空更快
B.进食能够有效增加药物在胃内的滞留时间
C.食物能够保证药物连续不断地进入肠道,增加了吸收量
D.食物刺激胆汁分泌,增加了药物的溶解度
E.食物增加了药物透过肠道上皮细胞的能力
参考答案:D
解析:
本题考查的是影响药物吸收的生理因素。
当原料药粒径较大时,进食时比空腹的Cmax、AUC都大,说明食物刺激胆汁分泌,增加了药物的溶解度。
第563题
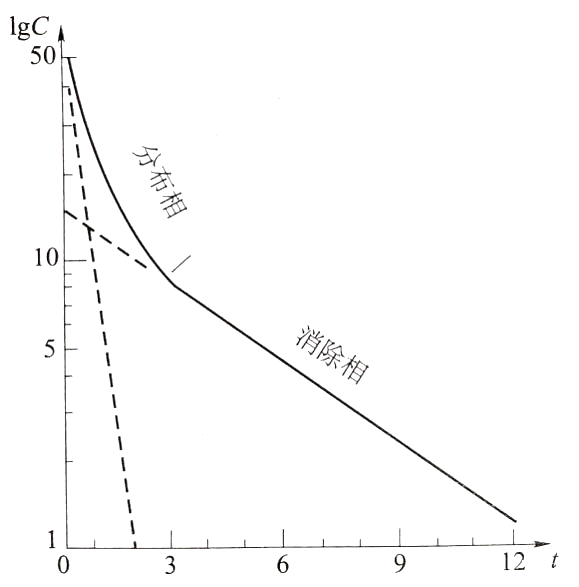
经计算,该药的体内血药浓度-时间曲线符合二室模型,其t1/2(α)为2.2小时,t1/2(β)为18.0小时,说明
A.该药在体内清除一半需要18.0小时
B.该药在体内清除一半需要20.2小时
C.该药在体内快速分布和缓慢清除
D.该药在体内基本不代谢
E.该药一天服用1次即可
参考答案:C
解析:
本题考查的是双室模型的特征。
双室模型具有分布相和消除相。t1/2(α)为2.2小时,说明快速分布,t1/2(β)为18.0小时,说明缓慢消除。
第564题
下列可以有效增加难溶性药物溶解度、提高生物利用度的方式中,不属于增加难溶性药物溶解度的方法是
A.制成固体分散体
B.合并使用膜渗透增强剂
C.制成盐
D.制成环糊精包合物
E.微粉化
参考答案:B
解析:
本题考查的是增加药物溶解度的方法。
增加药物溶解度的方法包括:加入增溶剂、加入助溶剂、制成盐类、使用混合溶剂、制成共晶。此外,提高温度、改变pH可促进药物的溶解;应用微粉化技术可减小粒径,促进药物溶解;固体分散体、包合技术等新技术的应用也可促进药物的溶解。
第565题
该药品处方组分中的“主药”应是
A.红霉素
B.青霉素
C.阿奇霉素
D.氧氟沙星
E.氟康唑
参考答案:D
解析:
本题考查的是考查氧氟沙星缓释胶囊处方分析。
氧氟沙星为主药。丸芯中枸橼酸为pH缓冲剂和渗透压调节剂;微晶纤维素和乳糖为稀释剂。包衣液处方中PEG6000为增塑剂,其用量不能过高,否则有致孔剂的作用,可加速药物释放;滑石粉为抗黏剂;Eudragit NE30D和Eudragit L30D-55为主要缓释包衣材;水为溶剂,十二烷基硫酸钠为稳定剂。
第566题
该制剂处方中Eudragit NE30D、Eudragit L30D-55的作用是
A.缓释包衣材料
B.胃溶包衣材料
C.肠溶包衣材料
D.肠溶载体
E.黏合剂
参考答案:A
解析:
本题考查的是考查氧氟沙星缓释胶囊处方分析。
氧氟沙星为主药。丸芯中枸橼酸为pH缓冲剂和渗透压调节剂;微晶纤维素和乳糖为稀释剂。包衣液处方中PEG6000为增塑剂,其用量不能过高,否则有致孔剂的作用,可加速药物释放;滑石粉为抗黏剂;Eudragit NE30D和Eudragit L30D-55为主要缓释包衣材;水为溶剂,十二烷基硫酸钠为稳定剂。
第567题
根据处方组分分析推测该药品的剂型是
A.缓释片剂
B.缓释小丸
C.缓释颗粒
D.缓释胶囊
E.肠溶小丸
参考答案:D
解析:
本题考查的是胶囊剂的举例。
由于处方中Eudragit NE30DEudragit L30D-55为缓释包衣材料,所以排除肠溶小丸。只有在胶囊剂里才提到空白丸核,所以答案选缓释胶囊。
第568题
该制剂的主药规格为0.2g,需要进行的特性检查项目是
A.不溶性微粒
B.崩解时限
C.释放度
D.含量均匀度
E.溶出度
参考答案:C
解析:
本题考查的是胶囊剂的质量要求。
溶出度与释放度测定法:溶出度系指活性药物从片剂、胶囊剂或颗粒剂等普通制剂在规定条件下溶出的速率和程度,在缓释制剂、控释制剂、肠溶制剂及透皮贴剂等制剂中也称释放度。缓释胶囊应符合缓释制剂的有关要求并应进行释放度检查。
第569题
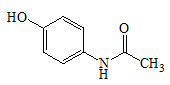
在体内发生代谢,生成“亚胺-醌”物质,已发毒性作用的药物是
A.
双氯芬酸

B.
奈法唑酮

C.
普拉洛尔
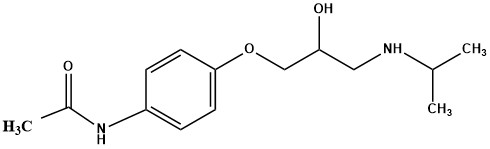
D.
苯噁洛芬
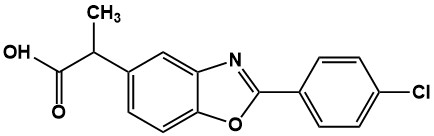
E.
对乙酰氨基酚
参考答案:ABCE
解析:
本题考查的是药物与体内代谢过程引发的毒副作用。
芳香胺由于在体内代谢时,易产生强亲电性亚胺-醌,表现出潜在的毒副作用,临床应用时需加小心。如双氯芬酸、对乙酰氨基酚、普拉洛尔、奈法唑酮等,长时间和大剂量服用易导致肝脏损伤。
第570题
竞争性拮抗药的特点有
A.使激动药的量效曲线平行右移
B.与受体的亲和力用pA2表示
C.与受体结合亲和力小
D.不影响激动药的效能
E.内在活性较大
参考答案:ABD
解析:
本题考查的是竞争性拮抗药。
拮抗药分为竞争性拮抗药和非竞争性拮抗药。竞争性拮抗药与受体也有很强的亲和力,但内在活性为零。由于激动药与受体的结合是可逆的,竞争性拮抗药可与激动药互相竞争与相同受体结合,产生竞争性抑制作用,可通过增加激动药的浓度使其效应恢复到原先单用激动药时的水平。竞争性拮抗药使激动药的量-效曲线平行右移,但其最大效应不变。竞争性拮抗药与受体的亲和力可用拮抗参数(pA2)表示。
第571题
关于生物等效性研究的说法,正确的有
A.生物等效性研究方法的优先顺序常为药代动力学研究、药效动力学研究、临床研究和体外研究
B.用于评价生物等效性的药动学指标包括Cmax和AUC
C.仿制药生物等效性试验应尽可能选择原研产品作为参比制剂
D.对于口服常释制剂,通常需进行空腹和餐后生物等效性研究
E.筛选受试者时的排除标准应主要考虑药效
参考答案:ABCD
解析:
本题考查的是生物等效性。
生物等效性是指在相似的试验条件下单次或多次给予相同剂量的试验药物后,受试制剂中药物的吸收速度和吸收程度与参比制剂的差异在可接受范围内。仿制药人体生物等效性试验以药物在人体内的药动学参数作为终点评价指标。生物等效性研究方法按照研究方法评价效力,其优先顺序为药代动力学研究、药效动力学研究、临床研究和体外研究。用于评价生物等效性的药动学指标包括Cmax和AUC。参比制剂的选择:仿制药生物等效性试验应尽可能选择原研产品作为参比制剂,以保证仿制药质量与原研产品一致。对于口服常释制剂,通常需进行空腹和餐后生物等效性研究。筛选受试者时的排除标准应主要基于安全性方面的考虑。故排除E。
第572题
药物引起脂肪肝的作用机制有
A.促进脂肪组织释放游离脂肪酸入肝过多
B.增加合成脂蛋白的原料如磷脂等
C.刺激肝内合成三酰甘油增加
D.破坏肝细胞内质网结构或抑制某些酶的合成导致脂蛋白合成障碍
E.损害线粒体,脂肪酸氧化能力下降,使脂肪在肝细胞内沉积
参考答案:ACDE
解析:
本题考查的是药物对机体各系统的毒性作用。
药物引起脂肪肝的作用机制有:①游离脂肪酸供应过多,某些肝脏毒物如DDT、尼古丁与肼类,甚至高血压病等,刺激垂体-肾上腺内分泌系统,通过使儿茶酚胺大量释放,导致脂肪组织释放游离脂肪酸入肝过多,最终形成脂肪肝;②三酰甘油合成增加,如异丙醇、巴比妥类可使肝内三酰甘油合成增加导致脂肪肝;③脂蛋白合成障碍,常由于合成脂蛋白的原料如磷脂或组成磷脂的胆碱等物质缺乏,或由于肝脏毒物(如酒精、四氯化碳或霉菌毒素)破坏内质网结构或抑制某些酶的活性,使脂蛋白及组成脂蛋白的磷脂、蛋白质合成发生障碍,以致不能将脂肪运输出去,造成脂肪在肝细胞内堆积;④脂肪酸氧化减少,如机体摄入大量乙醇后,损害线粒体,使线粒体肿胀,氧化磷酸化解偶联,ATP含量下降,脂肪酸氧化能力下降,脂肪在肝细胞内沉积。
第573题
需用无菌检查法检查的吸入制剂有
A.吸入气雾剂
B.吸入喷雾剂
C.吸入用溶液
D.吸入粉雾剂
E.吸入混悬液
参考答案:BCE
解析:
本题考查的是吸入制剂。
药物溶解或分散于合适介质中,以气溶胶或蒸汽形式递送至肺部发挥局部或全身作用的液体或固体制剂,可分为吸入气雾剂、吸入喷雾剂、吸入粉雾剂、吸入液体制剂、可转变为蒸汽的制剂,其中吸入喷雾剂和吸入液体制剂应为无菌制剂。吸入液体制剂包括吸入溶液、吸入混悬液、吸入用溶液(需稀释后使用的浓溶液)或吸入用粉末(需溶解后使用的粉末),吸入液体制剂使用前其pH应在3~10。
第574题
可用于除去溶剂中热原的方法有
A.吸附法
B.超滤法
C.反渗透法
D.离子交换法
E.凝胶过滤法
参考答案:ABCDE
解析:
本题考查的是热原的除去方法。
根据热原的基本性质和可能被污染的途径,除去药液中的热原可从以下两个方面着手。
1.除去药液或溶剂中热原的方法 ①吸附法②离子交换法③凝胶滤过法④超滤法⑤反渗透法⑥其他方法:采用两次以上湿热灭菌法,微波也可破坏热原。
2.除去容器或用具上热原的方法 ①高温法②酸碱法。
第575题
属于脂质体质量要求的控制项目有
A.形态、粒径及其分布
B.包封率
C.载药量
D.稳定性
E.磷脂与胆固醇比例
参考答案:ABCD
解析:
本题考查的是脂质体的质量要求。
脂质体的粒径大小及其分布、包封率、载药量和稳定性等可直接影响脂质体在体内的分布与代谢,最终影响疗效及毒副作用,因此需要密切关注并加以严格控制。除应符合《中国药典》有关制剂通则规定外,还需控制以下项目:1.形态、粒径及其分布2.包封率 3.载药量4.脂质体的稳定性。
第576题
关于标准物质的说法,正确的有
A.标准品是指采用理化方法鉴别、检查或含量测定时所用的标准物质
B.标准物质是指用于校准设备、评价测量方法、给供试药品赋值或鉴别药品的物质
C.标准品与对照品的特性量值均按纯度(%)计
D.我国国家药品标准物质有标准品、对照品、对照药材、对照提取物和参考品共五类
E.标准物质具有确定的特性量值
参考答案:BDE
解析:
本题考查的是标准物质。
标准物质系指供药品检验(鉴别、检查、含量或效价测定)中使用的,具有确定特性量值,用于校准设备、评价测量方法、给供试药品赋值或者鉴别用的物质。国家药品标准物质共有五类:标准品、对照品、对照药材、对照提取物、参考品,均应按其标签或使用说明书的规定使用和贮藏。其中,供化学药物与抗生素测定用的标准物质为对照品与标准品。对照品系指采用理化方法进行鉴别、检查或含量测定时所用的标准物质,其特性量值一般按纯度(%)计。例如,紫外-可见分光光度法测定药物含量时使用对照品作为标准物质;标准品系指用于生物检定或效价测定的标准物质,其特性量值按效价单位(U)或重量单位(μg)计,以国际标准物质进行标定,供试品的效价以标准品的效价单位赋值。例如,硫酸庆大霉素的含量限度,《中国药典》规定:按无水物计算,每1mg的效价不得少于590庆大霉素单位(1000庆大霉素单位相当于1mg庆大霉素)。
第577题
乳剂属于热力学不稳定体系,在放置过程中可能出现的不稳定现象有
A.分层
B.絮凝
C.转相
D.合并
E.酸败
参考答案:ABCDE
解析:
本题考查的是乳剂的稳定性。
乳剂属于热力学不稳定的非均相分散体系,制成后在放置过程中常出现分层、合并、破裂、絮凝、转相、酸败等不稳定的现象。
【考点延展】
乳剂的稳定性:
1.分层/乳析:可逆。分层的乳剂经振摇可重新分散。原因:分散相和分散介质间的密度差。
2.絮凝:乳滴电荷降低,ζ电位降低→可逆的聚集。原因:电解质、离子型乳化剂等。
3.合并:乳化膜部分破裂→液滴合并变大。
4.破裂:液滴合并后,进而使油水分离。不可逆。
破裂的原因:①微生物污染;②温度过高或过低;③加与乳化剂发生作用的物质。
5.转相:乳剂类型改变。原因:改变乳化剂性质或添加相反类型乳化剂。
6.酸败:由于外界因素、微生物影响,使油相或乳化剂变质。措施:加入抗氧剂、防腐剂。
第578题
作用于EGFR靶点,属于酪氨酸激酶抑制剂的有
A.埃克替尼
B.尼洛替尼
C.厄洛替尼
D.克唑替尼
E.奥希替尼
参考答案:ACE
解析:
本题考查的是靶向抗肿瘤药。
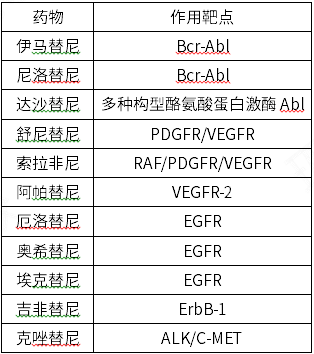
酪氨酸激酶抑制剂XX替尼,其中厄洛替尼、奥希替尼、埃克替尼的靶点是EGFR。
【考点延展】
第579题
某药物体内过程符合药物动力学单室模型药物消除按一级速率过程进行,静脉注射给药后进行血药浓度监测1h和4h时血药浓度分别为100mg/L和12.5mg/L,则该药静脉注射3h时的血药浓度是
A.75mg/L
B.50mg/L
C.25mg/L
D.20mg/L
E.15mg/L
参考答案:C
解析:
本题考查单室模型静脉注射给药。lgC=-kt/2.303+lgC0,把t=1,C=100;t=4,C=12.5代入公式中,可得斜率b=-0.3,结局a=2.3,所以回归方程为lgC=-0.3t+2.3.当t=3时,代入公式,可得C=25.
第580题
关于药物动力学参数表观分布容积(V)的说法正确的是
A.表观分布容积是体内药量与血药浓度间的比例常数,单位通常是L或L/kg
B.特定患者的表观分布容积是一个常数,与服用药物无关
C.表观分布容积通常与体内血容量有关,血容量越大,表观分布容积越大
D.特定药物的表观分布容积是一个常数,所以特定药物的常规临床剂量是固定的
E.亲水性药物的表观分布容积往往超过体液的总体积
参考答案:A
解析:
本题考查药动学参数。表观分布容积是体内药量与血药浓度间相互关系的一个比例常数。V=X/C。单位通常是L或L/kg。对于具体药物来说,V是个确定的值。